癌症之所以致命,原因之一是肿瘤细胞具有转移性。为了搞清楚它们是怎样侵袭和转移到健康的组织和器官上,我国科学家与美国科学家合作,利用微加工工艺在体外构建出了一种模拟肿瘤细胞侵袭的三维微环境。这一成果发表在日前出版的《美国国家科学院院刊》上。
在指甲大小的生物芯片上,构建三维微环境
成果的主要完成人、中科院物理所研究员刘雳宇介绍:“现有的癌症生物实验通常是在培养皿中进行的,但这是一个二维环境。而人体是一个三维环境,因此研究人员普遍都认为培养皿中的环境尚不足以模拟肿瘤细胞是如何侵袭健康组织和器官的。”
活体实验通常用小白鼠,一是成本高,二是时间长,三是培育难度较大。人体实验涉及许多伦理问题,更加难以开展。因此,科学家们提出一种设想——是否可以在体外构建一种与人体相似的、微小的三维环境。
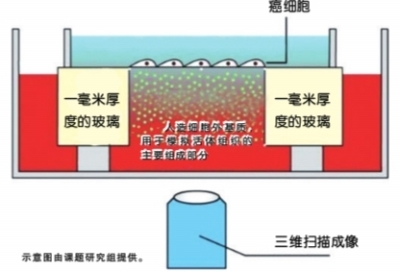
“这就用到了我们微加工和生物物理的技术了。”刘雳宇说,“我们在微流体和微加工上非常有优势。”这种生物芯片只有拇指指甲大小,但就是在这个“小东西”上,科学家们模拟出了与人类血管、胶原蛋白相似的三维微环境。“我们将癌症细胞放入这个芯片,就能观察到它们的活动过程和轨迹。”采用这种方式,还可以控制并改变微环境,对肿瘤细胞的侵袭生物行为进行较为精确的定量研究。
“当然,我们达不到与活体完全相似,这种微环境的模拟也不能取代活体实验。我们只是希望能够通过抓住主要的因素,模拟出肿瘤细胞生长和发展的基本条件,提供一条研究的新途径。”刘雳宇说。
发现肿瘤细胞或许存在博弈行为
利用这种新的方法,结合三维影像技术,“我们能够直观地看到侵袭细胞在三维空间中的具体位置,这是在简单二维环境下所不能得到的信息。”刘雳宇说,他们已经取得了一些成果。
“首先,我们发现葡萄糖等浓度梯度将诱导转移性肿瘤细胞侵袭三维外基质,而非转移性肿瘤细胞则不受影响,这与传统癌症理论结论相符。”刘雳宇介绍,癌症细胞也需要生长空间、营养等,当一个地方“供应不足”时,“它们必然向外扩散,这就导致了肿瘤细胞的转移。”
他们的第二个发现更为有趣。“我们发现,在肿瘤细胞的转移过程中,领头的细胞并不是固定的,而是你在前面一会,我在前面一会,周期性地替换。”刘雳宇说,“这就像在马拉松中使用的策略,如果一个运动员总是领跑克服风阻,体力消耗会非常大。因此,一个国家的运动员总是团结起来,你领跑一会,我领跑一会。”
这表明肿瘤细胞之间在侵袭组织的过程中可能存在着相互协作的博弈行为,而正是这种行为,让肿瘤细胞对健康组织的“入侵”更有效率。“这或许可以为癌症治疗提供一种新思路:阻碍或破坏肿瘤细胞之间的合作,让他们不合作,从而减缓侵袭和转移。”
第三个成果是发现了细胞群在侵袭过程中产生了力场。“我们原来猜测癌症细胞入侵时,基质应该是排斥的,就像跳水,跳进去时,水面应该是分开的。但实验结果证明,癌症细胞在入侵时,是在‘拉扯’细胞外基质,就像攀岩,是拉着岩面不断向上的。
“这些成果进一步证明了我们的思路是可行的。”刘雳宇说,他们的工作才刚刚起步。癌症细胞的侵入和转移分为三个步骤:“第一步,肿瘤破裂,癌症细胞溢出;第二步,癌症细胞侵入血管,并随着血液地流动开始转移;第三步,到达远端组织时,从新侵入组织开始复制、繁殖。”刘雳宇说:“我们现在的工作仅模拟了第一步,希望未来可以进一步模拟转移的微环境。我们物理所团队和北京大学医学院共同承担了一项973课题,希望未来五年可以通过与生物学家、病例学家更为紧密合作实现这一目标。(本报北京4月15日电 本报记者 齐 芳)



 上一版
上一版


 缩小
缩小 全文复制
全文复制